2018年,是中國(guó)生物制藥產(chǎn)業(yè)深化發(fā)展、信息技術(shù)加速賦能的關(guān)鍵一年。國(guó)家及各級(jí)地方政府圍繞產(chǎn)業(yè)創(chuàng)新、質(zhì)量提升與智能化轉(zhuǎn)型,密集出臺(tái)了一系列引導(dǎo)與支持政策,為產(chǎn)業(yè)發(fā)展構(gòu)筑了堅(jiān)實(shí)的政策框架。本文將對(duì)2018年國(guó)家層面及部分代表性省市的生物制藥產(chǎn)業(yè)主要政策,及其與信息系統(tǒng)集成服務(wù)的關(guān)聯(lián)進(jìn)行系統(tǒng)性匯總與分析。
一、 國(guó)家層面政策引領(lǐng)
國(guó)家層面的政策主要從宏觀戰(zhàn)略、審評(píng)審批、技術(shù)創(chuàng)新與產(chǎn)業(yè)融合等維度,為生物制藥產(chǎn)業(yè)指明了方向。
- 《“十三五”生物產(chǎn)業(yè)發(fā)展規(guī)劃》的深化落實(shí):雖然該規(guī)劃于2017年初發(fā)布,但其在2018年進(jìn)入全面深化落實(shí)階段。規(guī)劃明確提出加快發(fā)展精準(zhǔn)醫(yī)學(xué)新模式、推動(dòng)基因檢測(cè)和細(xì)胞治療等前沿技術(shù)發(fā)展,并對(duì)醫(yī)藥產(chǎn)業(yè)的數(shù)字化、智能化轉(zhuǎn)型提出要求,這為生物制藥與信息系統(tǒng)(如臨床數(shù)據(jù)管理、精準(zhǔn)醫(yī)療大數(shù)據(jù)平臺(tái))的集成奠定了基礎(chǔ)。
- 藥品審評(píng)審批制度改革持續(xù)推進(jìn):國(guó)家藥品監(jiān)督管理局(NMPA)在2018年繼續(xù)深化改革,優(yōu)化臨床試驗(yàn)審批程序,加快創(chuàng)新藥和臨床急需藥品上市。與之配套,對(duì)藥品全生命周期管理的信息化要求提升,《藥品數(shù)據(jù)管理規(guī)范》 等相關(guān)指南強(qiáng)調(diào)實(shí)驗(yàn)室信息管理系統(tǒng)(LIMS)、臨床試驗(yàn)電子數(shù)據(jù)采集(EDC)等信息系統(tǒng)必須符合數(shù)據(jù)完整性(ALCOA+原則)要求,推動(dòng)了合規(guī)、高效的信息系統(tǒng)集成服務(wù)在研發(fā)與生產(chǎn)環(huán)節(jié)的應(yīng)用。
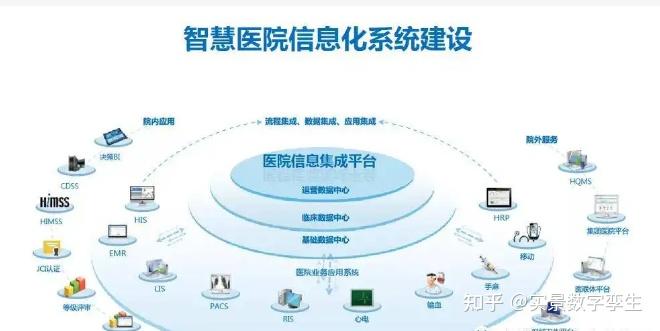
- 《關(guān)于促進(jìn)“互聯(lián)網(wǎng)+醫(yī)療健康”發(fā)展的意見》:由國(guó)務(wù)院辦公廳發(fā)布。此政策雖側(cè)重醫(yī)療服務(wù),但明確提出支持研發(fā)醫(yī)療人工智能輔助系統(tǒng)、探索智慧醫(yī)院建設(shè)、促進(jìn)健康醫(yī)療大數(shù)據(jù)發(fā)展。這直接拉動(dòng)了對(duì)生物制藥企業(yè)研發(fā)端(如真實(shí)世界研究數(shù)據(jù)平臺(tái))與營(yíng)銷端(數(shù)字化患者管理平臺(tái))的信息系統(tǒng)集成需求,促使藥企與IT服務(wù)商更緊密地合作。
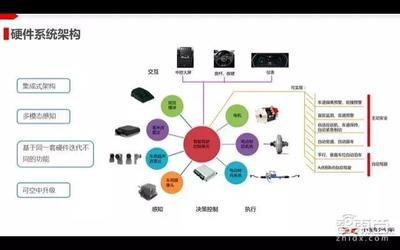
- 智能制造與工業(yè)互聯(lián)網(wǎng)相關(guān)政策:工信部等部門推動(dòng)的智能制造專項(xiàng)和工業(yè)互聯(lián)網(wǎng)發(fā)展行動(dòng)計(jì)劃,鼓勵(lì)醫(yī)藥行業(yè)建設(shè)智能工廠和數(shù)字化車間。這要求生物制藥企業(yè)將制造執(zhí)行系統(tǒng)(MES)、企業(yè)資源計(jì)劃(ERP)、過程控制系統(tǒng)(PCS)等進(jìn)行深度集成,實(shí)現(xiàn)生產(chǎn)過程的可視化、可控化和優(yōu)化,對(duì)提供跨平臺(tái)、高可靠性的信息系統(tǒng)集成服務(wù)商提出了更高要求。
二、 省市層面政策配套與特色發(fā)展
各省市結(jié)合自身產(chǎn)業(yè)基礎(chǔ),出臺(tái)了更具針對(duì)性的政策,并在信息化融合方面呈現(xiàn)不同特色。
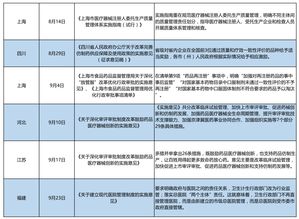
- 北京市:依托中關(guān)村和亦莊生物醫(yī)藥園等創(chuàng)新高地,北京政策強(qiáng)調(diào)原始創(chuàng)新與國(guó)際化。在《北京市加快科技創(chuàng)新發(fā)展醫(yī)藥健康產(chǎn)業(yè)的指導(dǎo)意見》中,明確提出推動(dòng)人工智能、大數(shù)據(jù)在新藥研發(fā)中的應(yīng)用,建設(shè)醫(yī)藥健康協(xié)同創(chuàng)新大數(shù)據(jù)平臺(tái)。其政策著力點(diǎn)在于促進(jìn)研發(fā)環(huán)節(jié)的IT與BT(生物技術(shù))融合,對(duì)高性能計(jì)算、AI藥物發(fā)現(xiàn)平臺(tái)等高端信息系統(tǒng)集成服務(wù)需求旺盛。
- 上海市:作為中國(guó)生物醫(yī)藥創(chuàng)新中心,上海在2018年持續(xù)優(yōu)化“張江藥谷”生態(tài)。其政策注重全產(chǎn)業(yè)鏈開放創(chuàng)新,在《促進(jìn)上海市生物醫(yī)藥產(chǎn)業(yè)高質(zhì)量發(fā)展行動(dòng)方案》相關(guān)部署中,強(qiáng)調(diào)建設(shè)生物醫(yī)藥產(chǎn)業(yè)地圖和智慧監(jiān)管服務(wù)平臺(tái)。這要求集成從研發(fā)、臨床、生產(chǎn)到流通的全程數(shù)據(jù)鏈,服務(wù)于產(chǎn)業(yè)規(guī)劃與精準(zhǔn)監(jiān)管,推動(dòng)了綜合性產(chǎn)業(yè)云平臺(tái)和物聯(lián)網(wǎng)集成解決方案的發(fā)展。
- 江蘇省:產(chǎn)業(yè)規(guī)模領(lǐng)先,政策聚焦于產(chǎn)業(yè)集群升級(jí)與制造智能化。例如,蘇州、泰州等地出臺(tái)政策,大力支持醫(yī)藥企業(yè)進(jìn)行智能化改造,對(duì)符合條件的信息化集成項(xiàng)目給予補(bǔ)貼。其需求側(cè)重于生產(chǎn)環(huán)節(jié)的自動(dòng)化控制系統(tǒng)集成、車間級(jí)物聯(lián)網(wǎng)部署以及供應(yīng)鏈協(xié)同平臺(tái)建設(shè),具有強(qiáng)烈的“工業(yè)互聯(lián)網(wǎng)+生物制藥”特征。
- 廣東省:依托粵港澳大灣區(qū)戰(zhàn)略,政策突出跨境合作與數(shù)字醫(yī)療。深圳、廣州等地鼓勵(lì)發(fā)展基因檢測(cè)、個(gè)性化醫(yī)療,并與信息技術(shù)產(chǎn)業(yè)優(yōu)勢(shì)結(jié)合,推動(dòng)健康醫(yī)療大數(shù)據(jù)中心建設(shè)。其政策環(huán)境催生了面向精準(zhǔn)醫(yī)療的IT-BT集成服務(wù),如集成基因測(cè)序、影像分析、電子病歷等多源數(shù)據(jù)的診療輔助系統(tǒng)。
三、 政策共性指向與對(duì)信息系統(tǒng)集成服務(wù)的影響
綜觀2018年各級(jí)政策,可以梳理出以下核心共性與影響:
- 主線一:鼓勵(lì)創(chuàng)新,提速研發(fā)。政策普遍鼓勵(lì)新藥創(chuàng)制,這直接增加了對(duì)藥物研發(fā)信息系統(tǒng)集成的需求,包括高性能計(jì)算集群、AI建模平臺(tái)、臨床試驗(yàn)一體化管理平臺(tái)(整合CTMS, EDC, eTMF等)的建設(shè)和整合。
- 主線二:提升質(zhì)量,嚴(yán)格監(jiān)管。隨著藥品上市許可持有人制度全面推行和國(guó)際標(biāo)準(zhǔn)接軌,對(duì)藥品生產(chǎn)質(zhì)量管理規(guī)范的要求空前嚴(yán)格。這迫使企業(yè)必須實(shí)施或升級(jí)符合GMP/GXP規(guī)范的質(zhì)量管理系統(tǒng)集成,確保從實(shí)驗(yàn)室到生產(chǎn)的全過程數(shù)據(jù)可靠、可追溯。
- 主線三:推動(dòng)智能制造,升級(jí)產(chǎn)業(yè)模式。無論是國(guó)家“中國(guó)制造2025”還是地方產(chǎn)業(yè)升級(jí)計(jì)劃,都將生物制藥列為智能制造重點(diǎn)領(lǐng)域。這帶來了對(duì)工業(yè)級(jí)信息系統(tǒng)集成的規(guī)模化需求,即實(shí)現(xiàn)設(shè)備層、控制層、管理層乃至企業(yè)層數(shù)據(jù)的無縫流通,構(gòu)建數(shù)字孿生工廠。
- 主線四:促進(jìn)數(shù)據(jù)驅(qū)動(dòng),拓展健康生態(tài)。“互聯(lián)網(wǎng)+醫(yī)療健康”政策促使藥企角色從“藥品提供商”向“健康解決方案伙伴”延伸。這要求企業(yè)集成內(nèi)部研發(fā)生產(chǎn)數(shù)據(jù)與外部醫(yī)療機(jī)構(gòu)、患者數(shù)據(jù),構(gòu)建患者管理平臺(tái)或真實(shí)世界證據(jù)平臺(tái),對(duì)跨組織、跨安全域的系統(tǒng)集成能力提出挑戰(zhàn)。
結(jié)論:2018年的政策體系清晰地表明,中國(guó)生物制藥產(chǎn)業(yè)的發(fā)展已與信息化、智能化進(jìn)程深度綁定。信息系統(tǒng)集成服務(wù)已不再是單純的IT支持,而是成為保障藥品安全、提升研發(fā)效率、實(shí)現(xiàn)智能制造和開拓新商業(yè)模式的核心賦能工具。政策不僅創(chuàng)造了廣闊的市場(chǎng)需求,也引導(dǎo)著集成服務(wù)向更專業(yè)(懂醫(yī)藥法規(guī))、更深入(觸及核心工藝)、更融合(BT與IT深度融合)的方向演進(jìn)。對(duì)于生物制藥企業(yè)和信息系統(tǒng)集成服務(wù)商而言,精準(zhǔn)理解并順應(yīng)這一政策趨勢(shì),是把握未來發(fā)展機(jī)遇的關(guān)鍵。